Die wachsende Menge an Daten und die zunehmende Komplexität von Künstlicher Intelligenz (KI) und Machine Learning (ML) in Verbindung mit modernster Rechenleistung werden die Entwicklung von Medikamenten und Therapien bahnbrechend verändern. Die FDA (U.S. Food and Drug Administration) hat dazu 2023 zwei Discussion Paper veröffentlicht, die den Einsatz von KI/ML bei der Produktion von Pharmazeutika diskutieren, denn:
Der schon länger existierende KI/ML-Leitfaden der FDA für Medizinprodukte ist für adaptive KI-Technologien nicht geeignet.
Das bedeutet, dass KI/ML nicht nur im Vorfeld von den Herstellungsverfahren benötigt wird, sondern auch während der Produktion. So können die Herstellungsprozesse immer auf die aktuellen Konditionen angepasst werden.
Die FDA, die IHC (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use) und auch die lokale Behörden wie das Bundesministerium für Gesundheit veranstalten zu dem Thema regelmäßig Workshops, in denen IT – Fachpersonal, Pharmaindustrie, Regulierungsbehörden, akademische Gruppen und andere daran arbeiten wie KI und ML am besten im gesamten Prozess der Arzneimittelentwicklung eingesetzt werden können.
Aber was ist KI/ML?
KI kann allgemein als der Querschnitt der Informatik, der Mathematik und des Ingenieurwesens beschrieben werden, der Algorithmen oder der Modelle verwendet, um die Aufgaben zu erfüllen und die Verhaltensweisen wie das Lernen, das Entscheiden und das Vorhersagen treffen kann. ML wird als eine Untergruppe der KI betrachtet. Die ML-Modelle können durch die Analyse von Daten entwickelt werden, ohne dass die Modelle explizit programmiert werden. Außerdem gibt es eine Vielzahl von ML-Methoden und verschiedene Arten von Algorithmen, die je nach Fall eingesetzt werden können.
Der aktuelle Einsatz von KI/ML in der Pharmaindustrie
In der Forschung (R&D – Research and Development) wird KI/ML schon weitgehend eingesetzt, um z.B. die ideale Wirkstoffkandidaten zu screenen oder die Wirksamkeit von den Substanzen vorherzusagen, bevor sie produziert werden. Das spart überflüssige Tests, Ressourcen und Zeit. Außerdem kann ML zusammen mit der statistischer Versuchsplanung und dem digitalen Zwilling (DoE-Design of Experiments und dem Digital Twin) zur Prozessoptimierung eingesetzt werden, um die idealen Produktionsverfahren für die Wirkstoffe zu etablieren. Um das Verhalten von den Wirkstoffkandidaten im Körper oder in der Kombination mit anderen Wirkstoffen vorherzusehen, werden die molekulare Modellierung und die computerbasierte Biologie generell (Molecular Modelling und Computational Biology) beim Design neuer Wirkstoffe (Drug Design) bereits eingesetzt.
… und in Zukunft?
KI/ML kann dazu beitragen, dass sichere, wirksame und qualitativ hochwertige Behandlungen schneller zur Verfügung stehen. Die FDA schreibt, dass KI-Technologien für die Arzneimittelherstellung wichtig sind, da sie die Prozesskontrolle verbessern, Frühwarnsignale erkennen und Produktverluste verhindern können.
Bisher wurden Hochdurchsatzexperimente nur im Forschungsbereich angewendet, mit Entwicklung von hochpräzisen Therapien, die weit über das Verständnis der personalisierten Medizin hinaus gehen, sollte sich das ändern.
Immer mehr Wirkstoffe werden biotechnologisch hergestellt – als Biologicals. Um die richtigen Herstellungsverfahren zu finden, wird im Screening, also mit Hilfe von unzähligen Vorversuchen, KI/ML angewendet. Das ist bei der finalen Produktion aber nicht erlaubt.
Es erfordert eine sehr komplexe Regelungstechnik, um Screening – Experimente, also Verfahren, in denen hunderte Experimente gleichzeitig ablaufen, zu steuern. Gerade der Verlauf von biologischen Kultivierungen muss unter ständiger Beobachtung erfolgen. Ist die Dichte der Zellen ok? Stimmt die Temperatur? Sollte noch mehr Nährlösung zugefüttert werden? Und irgendwann wird die perfekte Hefe und Rührgeschwindigkeit usw. gefunden, um den Wirkstoff bestmöglich herzustellen.
Bei der Optimierung von Herstellungsprozessen für Wirkstoffe wie z.B. dem Insulin läuft es schon ähnlich ab.
Bei der Herstellung von Biologicals ist der Einsatz von „Black Box Modellen“ wie Neuronalen Netzen bisher nicht erlaubt. Aber vielleicht braucht man diese nur zur Prozessoptimierung und kann sich bei der Herstellung auf nachvollziehbare Algorithmen beschränken?
Wenn nachhaltige und hoch präzise Therapien für die High – Precision – Medicine eine Zukunft haben sollen, muss aber sowohl in der Diagnostik als auch bei Herstellung KI/ML eingesetzt werden, um die vielen notwendigen Experimente und Prozesse zu steuern.
High Precision Medicine – die Zukunft
Bei der Steuerung von Hochdurchsatz Prozessen, wie sie z.B. in der High-Precision Medicine eine Rolle spielen werden, ist eine manuelle Steuerung nicht möglich. Das bedeutet, es ist nur durch eine automatisierte Regelung mit Einsatz von ML möglich, 100e Bio-Reaktoren zu kontrollieren. Ergebnisse von Messungen, Sensoren oder Assays können ohne ML nicht korrekt und v.a. nicht rechtzeitig ausgelesen und ausgewertet werden.
Ein Beispiel hierfür ist z.B. die Bewertung von komplexen Spekten oder die Vorhersage von Konzentrationen, die nur durch zeitraubende Enzym–gekoppelte Assays ermittelt werden können.
Wie ist der Stand der FDA zum Einsatz von KI/ML in der Produktion von biologisch basierten Medikamenten?
Die Intelligente Produktion und die Integration des maschinellen Lernens, einschließlich der molekularen Modellierung in der Biotechnologie und ihres Nutzens für die Umwelt, werden in den jüngsten Veröffentlichungen erörtert.
Der Einsatz von Modellen beschleunigt die Zeit, mit der Medikamente an den Markt kommen, macht die Herstellungsverfahren effizienter und damit auch ökologischer und unterstützt somit nachhaltige Geschäftsmodelle in allen Richtungen.
Im Discussion Paper: Artificial intelligence in drug manufacturing werden die Möglichkeiten von AI/ML in Herstellungsprozessen genannt und erklärt.
Zunächst wurde definiert, in welchen Bereichen und wie AI/ML in der Produktion angewendet werden können: Die Verwendung von Cloud-Anwendungen können die Überwachung von Daten und Aufzeichnungen in der pharmazeutischen Produktion beeinträchtigen. Das Internet der Dinge (IoT) kann die Menge, der bei der pharmazeutischen Herstellung erzeugten Daten erhöhen und die bestehenden Datenverwaltungspraktiken beeinträchtigen. Kontinuierlich lernende KI-Systeme, die sich an Echtzeitdaten anpassen, können eine Herausforderung für die behördliche Bewertung und Überwachung darstellen – hier wird es interessant, ob sich die Modelle weiterentwickeln dürfen, wenn neue Informationen verfügbar werden. Derzeit ist dies in den Leitlinien für Medizinprodukte nicht erlaubt.
Weiterhin benötigen die Produktionsfirmen Klarheit darüber, ob und wie die Anwendung von KI in der pharmazeutischen Produktion der behördlichen Aufsicht unterliegt und ob sie möglicherweise Standards für die Entwicklung und Validierung von KI-Modellen benötigen, die für die Prozesskontrolle notwendig sind, sowie Standards zur Unterstützung von Freigabetests.
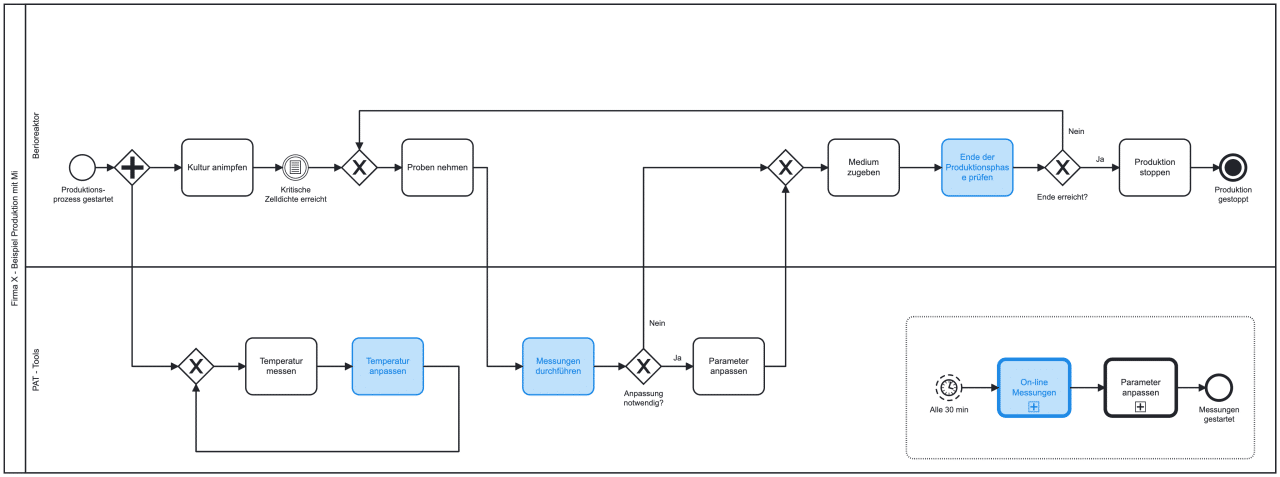
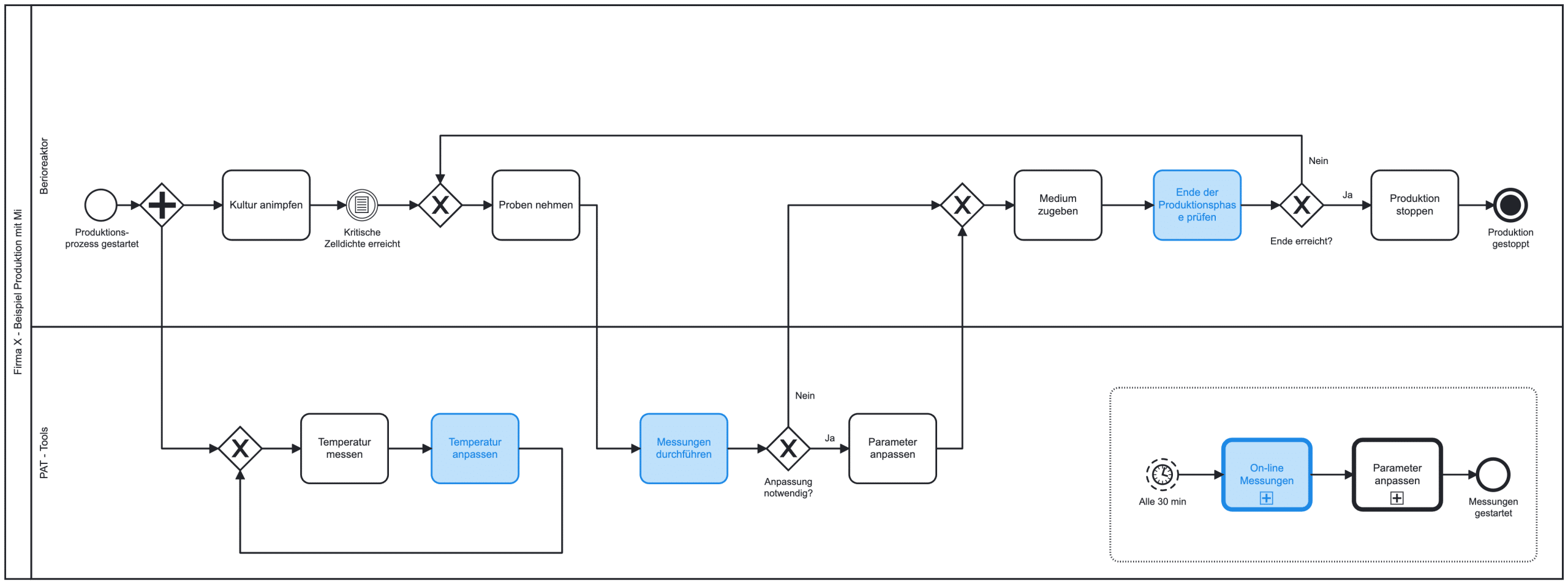
Vereinfachte BPMN-Darstellung eines Produktionsprozess, mit blau markierten Aktivitäten, bei denen ML jetzt schon eine tragende Rolle spielen kann: z.B. bei der Vorhersage wichtiger, nicht sofort messbarer Prozessparameter wie dem PH – Wert.